沉默的代償與系統性失序:高胰島素血症的病理進程
| ◄ 返回 |
| 發佈日期:2026/01/27 |
沉默的代償與系統性失序:高胰島素血症的病理進程在傳統代謝疾病的臨床診斷中,血糖升高往往被視為疾病的開端;然而,在分子生物學的真實軌跡裡,「高胰島素血症」(Hyperinsulinemia)才是隱藏在水平面下的巨大冰山。它是身體在面對能量過載時,所採取的一種長期、疲勞且具毀滅性的代償策略。 一、 分子機制:從「代償性分泌」到「受體後脫敏」當細胞產生胰島素阻抗時,胰島 $\beta$ 細胞會感應到葡萄糖清除率下降,進而透過旁分泌與內分泌回饋機制,大幅增加胰島素的合成與釋放。這種「代償性高胰島素血症」在初期能維持血糖在正常範圍,但卻在分子層級埋下了連鎖崩解的伏筆:
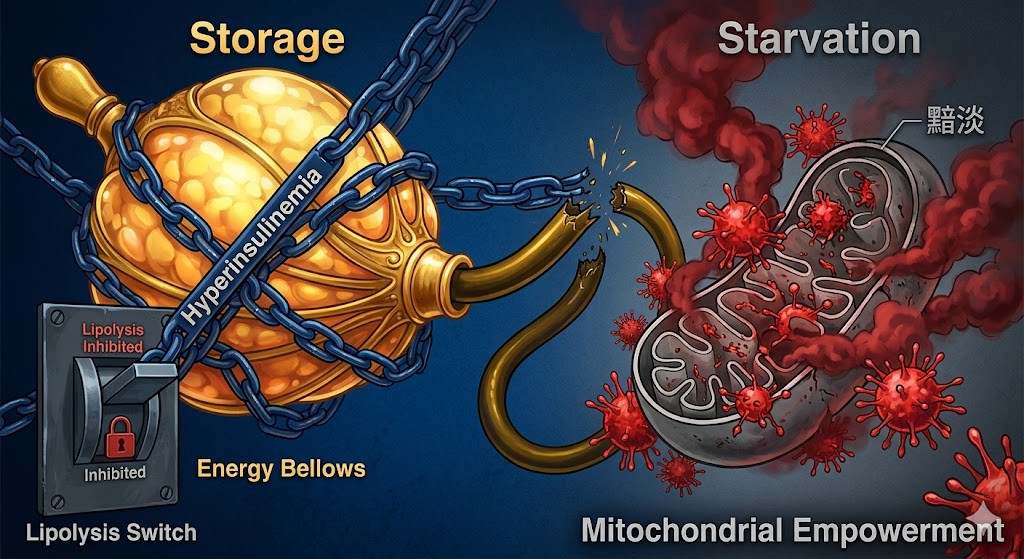
二、 生物哲學:儲能鎖定與熱力學的囚徒從生物哲學的角度看,胰島素是人體最強大的「儲能指令」。當血液中充斥著高濃度的胰島素時,身體的「燃脂開關」(脂肪分解作用,Lipolysis)會被強力關閉。 高胰島素血症實質上將生物體鎖定在一個「只能儲存、無法提取」的熱力學囚籠中。 即使個體體脂肪極高,細胞內部卻可能因為無法切換至脂肪氧化模式而感受「能量飢餓」。這種狀態下,粒線體失去了代謝靈活性(Metabolic Flexibility),被迫長期依賴效率低下的無氧醣解或受損的氧化磷酸化。這不只是生化數據的異常,更是生物體失去了與環境能量波動同步的韌性。 三、 系統性衝擊:超越血糖的致病力高胰島素血症對器官的損害遠早於糖尿病的確診:
四、 臨床對策:精準降低生物指令強度逆轉代謝症候群的關鍵,不在於「控制血糖」,而在於「調降循環胰島素水平」:
|
  |

