能量秩序的崩解:胰島素阻抗的分子機制與生物哲學思辨
| ◄ 返回 |
| 發佈日期:2026/01/18 |
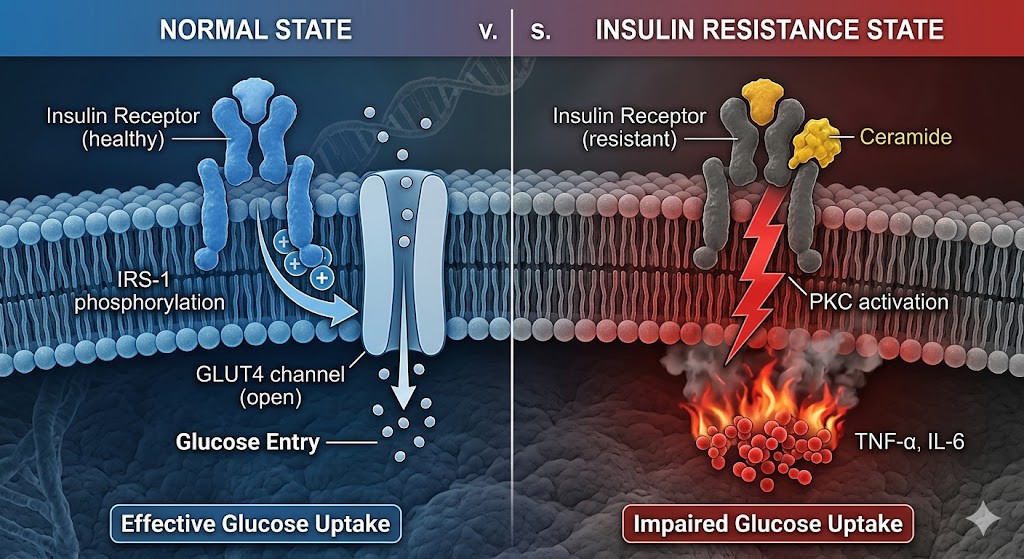
能量秩序的崩解:胰島素阻抗的分子機制與生物哲學思辨在代謝症候群的病理進程中,「胰島素阻抗」並非單一器官的失調,而是生物體在能量過載(Energy Overload)壓力下,為了維持細胞穩態(Homeostasis)所產生的病理性補償反應。 一、 分子生物學:受體後的訊號傳導失靈胰島素阻抗的核心在於胰島素受體(Insulin Receptor)及其下游訊號傳導通路的受損。當胰島素與細胞膜上的受體結合時,正常情況下會觸發一系列磷酸化反應,最終導致葡萄糖轉運蛋白(GLUT4)轉位至細胞膜。 但在現代代謝壓力下,這一機制受到以下多重打擊:
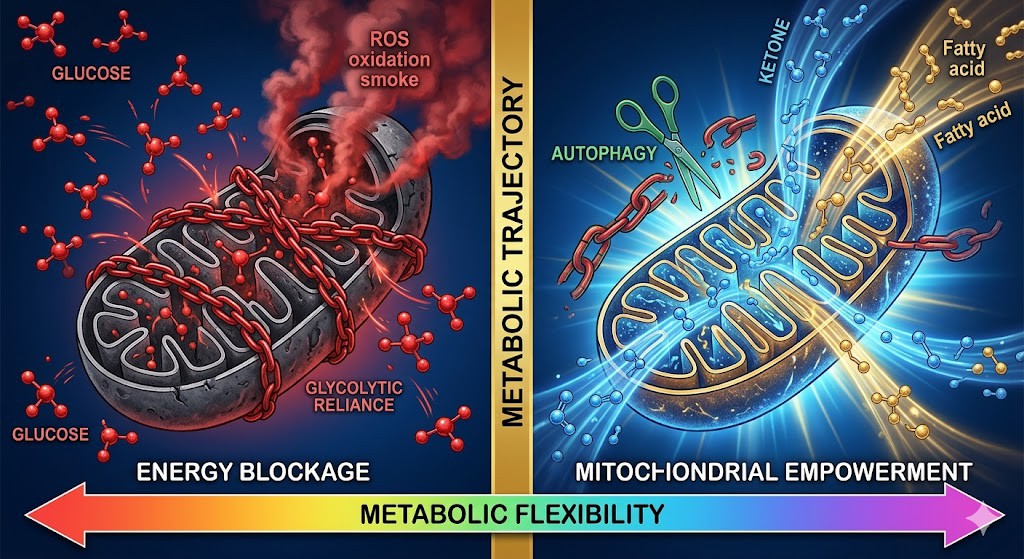
二、 生物哲學:保護性阻抗與熱力學悲劇從生物哲學的角度看,胰島素阻抗是細胞在熱力學第二定律下的自我防禦。當細胞內部粒線體(Mitochondria)的氧化壓力過大,無法處理更多底物時,細胞必須關閉入口以防止活性氧類(ROS)造成的毀滅性損傷。 阻抗,本質上是細胞拒絕「過度獲得」的生存意志。 分子醫學教授指出,現代醫學過度關注血糖這項「結果」,卻忽略了胰島素水平這項「成因」。高血糖僅是溢出的現象,真正的病灶在於全身性的高胰島素環境。這導致身體長期鎖定在「儲能模式」,脂肪氧化(Fat Oxidation)被完全抑制,粒線體的代謝靈活性(Metabolic Flexibility)消失,最終導致系統性的崩潰。 三、 臨床逆轉路徑:代謝軌跡的重構要逆轉胰島素阻抗,必須從「減少需求」與「增加消耗」雙管齊下:
結語:回歸生物體的秩序平衡胰島素阻抗不是一種「缺乏」,而是一種「過剩」導致的失能。管理代謝症候群的真諦,不在於研發更強效的降糖藥,而在於理解細胞的生物哲學限制,透過生活型態的精準介入,將身體從病理性的補償狀態,引導回歸有序的能量代謝。 |
  |

