分子層級的連鎖反應:胰島素阻抗與慢性低度發炎的惡性循環
在生物哲學的能量邏輯中,代謝與免疫本是同根同源。當細胞因胰島素阻抗(IR)而失去能量秩序時,身體便會啟動一種原始的防禦機制——慢性低度發炎(LSI)。這並非突發的紅腫熱痛,而是一場安靜且持久的分子侵蝕。
一、 分子機制:脂肪組織的免疫化
胰島素阻抗不僅發生在肌肉,更發生在脂肪組織中。當脂肪細胞因代償性高胰島素血症而過度肥大,會引發一系列免疫代謝的劇變:
-
脂肪細胞的缺氧與凋亡:
肥大的脂肪細胞因遠離血管微循環而陷入局部缺氧,這會激活缺氧誘導因子(HIF-1$\alpha$),進而釋放大量的趨化因子,召喚巨噬細胞浸潤。
-
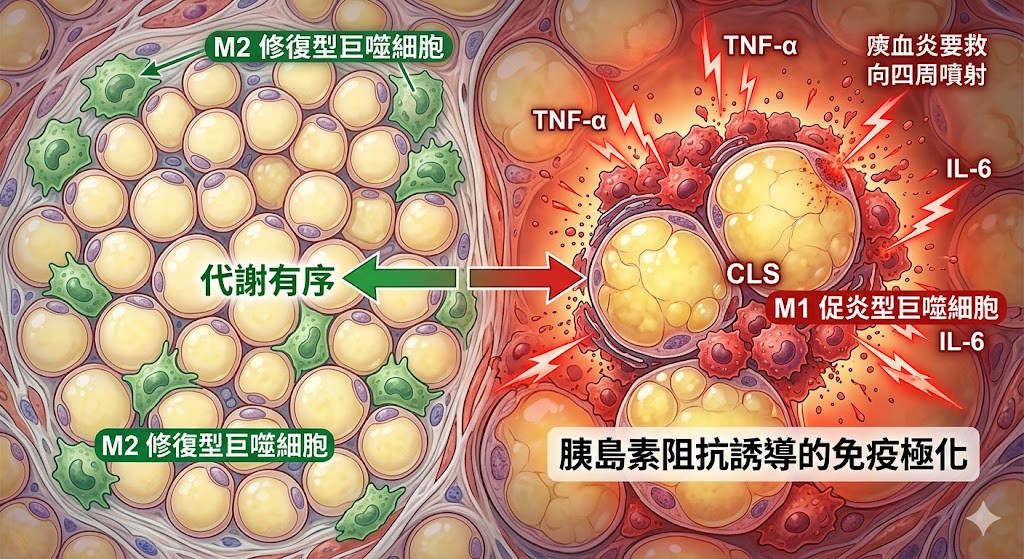
M1 型巨噬細胞的極化:
在胰島素阻抗的環境下,浸潤的巨噬細胞會從修復型的 M2 型轉變為促炎型的 M1 型。這些免疫細胞圍繞在凋亡的脂肪細胞周圍,形成所謂的「皇冠狀結構(CLS)」,並持續分泌 TNF-$\alpha$、IL-6 等發炎細胞因子。
-
NF-$\kappa$B 通路的持續激活:
這些發炎因子會透過細胞膜受體,激活胞內的 NF-$\kappa$B 轉錄因子,進而抑制胰島素受體底物(IRS-1)的磷酸化。這意味著:發炎直接導致了阻抗,而阻抗又進一步加劇了發炎。
二、 生物哲學:當「防禦」變成了「內耗」
從熱力學的角度看,發炎本是身體為了清除異常、恢復秩序的能量投入。然而,當胰島素阻抗鎖定了能量提取路徑時,細胞便陷入了「飢餓中的防禦」。
全身性發炎,實質上是生物體在無法有效管理能源時,所產生的「代謝摩擦」。
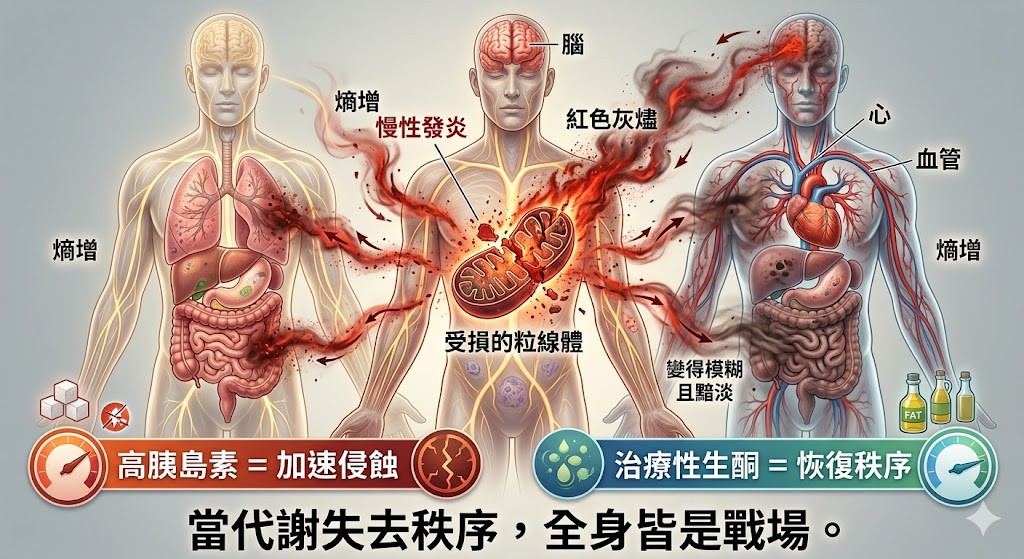
這種摩擦會導致粒線體的電子傳遞鏈效率下降,產生更多的活性氧(ROS),進而損傷血管內皮、破壞血腦屏障,將局部的代謝問題擴散為全身性的組織老化(Inflammaging)。這是一場生物秩序的「熵增」悲劇:為了自保而啟動的發炎,最終卻成了摧毀穩態的推手。
三、 臨床預警與干預:熄滅分子之火
要切斷這場連鎖反應,不能僅靠消炎藥,必須從「能源秩序」下手:
-
動態胰島素阻抗檢測 IRCT 的指標意義:
IRCT 能捕捉到身體在面臨能源波動時的代償強度。高阻抗讀數往往預示著潛在的發炎水平。透過調降胰島素需求,我們能減少 M1 型巨噬細胞的活化,從底層熄滅火源。
-
治療性生酮與抗炎環境:
酮體($\beta$HB)本身就是一種強力的内源性抗炎信號。它能抑制 NLRP3 炎性小體的活化,降低 IL-1$\beta$ 等致病因子的產出,為受損的組織提供一個修復的生化窗口。
-
HALA 哲學的實踐:
透過調整呼吸節律與降低壓力荷爾蒙(皮質醇),我們能抑制交感神經過度興奮引發的發炎級聯反應,讓免疫系統回歸「監控」而非「攻擊」狀態。
|